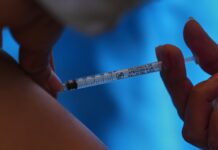
Amerykańska Agencja ds. Żywności i Leków (FDA) odrzuciła wniosek firmy Moderna dotyczący nowej szczepionki mRNA przeciwko grypie, co rodzi pytania o przyszłość rozwoju szczepionek i spójność przepisów w Stanach Zjednoczonych. Pomimo wcześniejszych wezwań FDA do kontynuowania projektu, agencja potrzebuje obecnie więcej danych przed rozpatrzeniem wniosku, co może opóźnić lub nawet zatrzymać wprowadzenie potencjalnie skuteczniejszej szczepionki przeciw grypie.
Przeszkody regulacyjne i zmieniające się standardy
Odmowa FDA wynika z oceny agencji, że badania kliniczne Moderny nie spełniały jej standardów. W szczególności w badaniach porównywano szczepionkę firmy Moderna ze standardowymi szczepionkami przeciw grypie, a nie z dużymi dawkami zwykle zalecanymi osobom z grupy wysokiego ryzyka. Chociaż firma Moderna porównywała swoją szczepionkę ze szczepionką zawierającą duże dawki u osób starszych i standardową dawką u młodszych osób, FDA upiera się, że porównanie ze standardem wyjściowym jest niewystarczające.
Decyzja jest niezwykła, ponieważ wydaje się nakładać nowy wymóg bez publicznego ogłoszenia i konsultacji. Prawnicy tacy jak Dorit Reiss z prawa Uniwersytetu Kalifornijskiego w San Francisco argumentują, że posunięcie FDA „stwarza realne ryzyko, że w przyszłym roku nie będziemy mieli tradycyjnych szczepionek” i odstrasza inwestycje w przyszły rozwój szczepionek przeciw grypie.
Technologia mRNA i ewolucja grypy
Szczepionka firmy Moderna wykorzystuje technologię informacyjnego RNA (mRNA), która wykazała potencjał szybszej adaptacji i prawdopodobnie lepszej ochrony przed szybko rozwijającymi się wirusami, takimi jak grypa. Produkcja tradycyjnych szczepionek przeciw grypie na bazie jaj zajmuje miesiące i nie zawsze skutecznie dopasowują się do krążących szczepów. Zdolność do szybkiego dostosowania szczepionek ma kluczowe znaczenie, biorąc pod uwagę potencjał pandemiczny grypy, co czyni tę decyzję jeszcze bardziej niepokojącą.
Obawy dotyczące zmian zasad
Odmowa FDA wynika z szerszych zmian w polityce szczepień pod rządami Trumpa. W styczniu urzędnicy ograniczyli zalecenia dotyczące rutynowych szczepień dzieci, w tym szczepionek przeciw grypie. To najnowsze posunięcie, w połączeniu z wewnętrznymi dyskusjami w FDA na temat zmiany ram przeglądu szczepionek, wskazuje na możliwą tendencję w kierunku bardziej rygorystycznych i nieprzewidywalnych przeglądów regulacyjnych.
Decyzja agencji nie była podyktowana względami bezpieczeństwa ani skuteczności: Dyrektor generalny Moderny, Stephane Buncell, stwierdził, że w swojej odmowie FDA nie stwierdziła żadnych problemów związanych z samą szczepionką. Zamiast tego list odmowny podpisany przez dyrektora Centrum Oceny i Badań Biologicznych (CBER) wymaga dodatkowych, nieokreślonych danych.
Globalne zatwierdzenie sprzeciwia się polityce Stanów Zjednoczonych
Warto zauważyć, że aplikacja Moderny jest obecnie rozpatrywana w Unii Europejskiej, Kanadzie i Australii. Ta różnica uwypukla rosnący rozdźwięk pomiędzy praktykami regulacyjnymi w Stanach Zjednoczonych i innych krajach rozwiniętych. Sytuacja podkreśla kruchość rozwoju szczepionek w Stanach Zjednoczonych.
Odmowa FDA sygnalizuje możliwe zaostrzenie standardów zatwierdzania szczepionek przeciwko chorobom układu oddechowego, bez przejrzystości i wyjaśnień. Ta nieprzewidywalność stwarza ryzyko dla zdrowia publicznego i może stłumić innowacje w krytycznym obszarze zapobiegania grypie.